Циклоалканы - это класс органических соединений, в которых молекула содержит один или несколько циклических углеродных скелетов, состоящих только из атомов углерода и водорода. Они являются частным случаем алифатических углеводородов и имеют важное значение в органической химии.
Циклоалканы можно классифицировать по размеру кольца. Наименьшим представителем этого класса является циклопропан, в котором углеродный скелет состоит из трех атомов углерода. Более крупные циклоалканы включают циклобутан, циклопентан, циклогексан и так далее. Существуют также ациклические изомеры, включающие два или более циклических скелета.
Номенклатура циклоалканов основана на правилах Международного союза по чистой и прикладной химии (IUPAC). Основное правило состоит в том, что название должно указывать на число атомов углерода в кольце и оканчиваться на суффикс "-ан". Например, циклопентан содержит пять атомов углерода в кольце, а циклогексан содержит шесть атомов углерода.
Электронное строение циклоалканов определяется сплошными и пунктирными линиями, представляющими связи между атомами углерода и атомами водорода. Также можно использовать символы двойной и тройной связи для указания наличия соответствующих связей. Например, циклопентан имеет формулу C5H10 и электронное строение, где каждый атом углерода соединяется с двумя атомами водорода и остальными атомами углерода через одинарные связи.
Циклоалканы подвержены различным видам напряжений, связанным с ограниченной подвижностью атомов углерода в кольце. Напряжение может быть вызвано углом при соединении двух атомов углерода, изогнутостью кольца или углобы в плоскости колец. Эти виды напряжения влияют на физические и химические свойства циклоалканов и могут вызывать нестабильность и реакционную активность соединений.
Определение и классификация циклоалканов
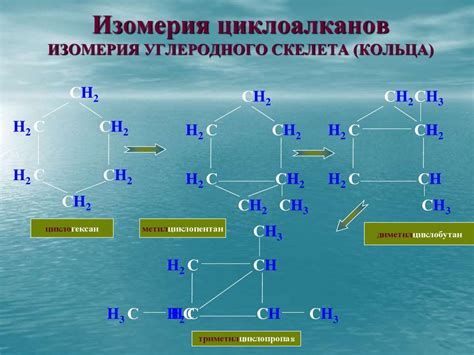
Циклоалканы - это класс органических соединений, которые содержат замкнутую ациклическую структуру из углеродных атомов, называемых алициклическими соединениями. Главной характеристикой циклоалканов является наличие одной или нескольких ациклических цепей, состоящих из углеродных атомов, формирующих кольцевую структуру.
Циклоалканы можно классифицировать по количеству углеродных атомов в кольце и типу связей между атомами:
- Наименьший циклоалкан - циклопропан, содержит три углеродных атома в кольце. Его структурная формула C3H6.
- Циклобутан - содержит четыре углеродных атома в кольце. Его структурная формула C4H8.
- Циклопентан - содержит пять углеродных атомов в кольце. Его структурная формула C5H10.
- Циклогексан - содержит шесть углеродных атомов в кольце. Его структурная формула C6H12.
- Циклогептан - содержит семь углеродных атомов в кольце. Его структурная формула C7H14.
Общая формула для циклоалканов с n углеродными атомами в кольце можно записать как CnH2n. Эта формула позволяет определить общую формулу для всех циклоалканов.
Номенклатура циклоалканов основывается на системе префиксов, которые указывают на количество углеродных атомов в кольце, и суффиксов, которые указывают на тип связи между углеродными атомами.
Циклоалканы имеют электронное строение, похожее на алканы, с различными напряжениями, связанными с кольцевыми структурами. Напряжения могут быть углеводородными или ариловыми, и они могут влиять на физические и химические свойства циклоалканов.
| Циклоалкан | Структурная формула | Общая формула |
|---|---|---|
| Циклопропан | H H | C3H6 |
| Циклобутан | H H H | C4H8 |
| Циклопентан | H H H H | C5H10 |
| Циклогексан | H H H H H | C6H12 |
| Циклогептан | H H H H H H | C7H14 |
Изомерия циклоалканов и их особенности
Циклоалканы – это насыщенные углеводороды, представляющие собой углеводородные цепи, образующие замкнутые кольца. Изомерия циклоалканов возникает из-за того, что в кольце может быть различное количество атомов углерода и, соответственно, различное количество валентных и свободных соединений.
Изомерия циклоалканов подразделяется на две основные группы: структурную и геометрическую.
- Структурная изомерия возникает из-за различной последовательности связей углеродных атомов в кольце. В результате этого возможны различные изомеры.
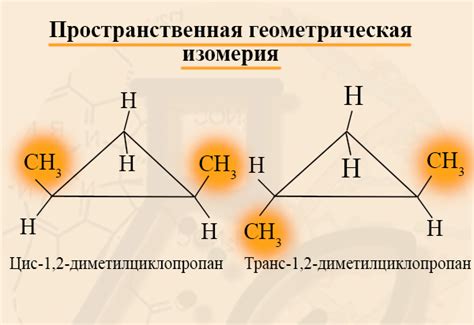
- Геометрическая изомерия возникает из-за различного пространственного расположения атомов.
Другими словами, структурная изомерия описывает различные варианты расположения связей в молекуле, а геометрическая изомерия описывает различия в пространственной конфигурации молекулы.
Структурная изомерия может быть представлена следующими видами:
- Изомерия циклопропана и циклобутана – циклопропан состоит из трех атомов углерода, которые образуют одинаковые связи (угол между связями составляет 60 градусов), тогда как циклобутан состоит из четырех атомов углерода с различными углами между связями.
- Изомерия циклопентана – циклопентан может принимать две структуры: плоскую и навесную. В случае плоской структуры все атомы располагаются в одной плоскости, а в случае навесной структуры один атом углерода располагается над или под плоскостью остальных атомов.
- Изомерия циклогексана – циклогексан подвержен геометрической и структурной изомерии. Геометрическая изомерия возникает из-за различного расположения атомов в положениях смежных кольца, а структурная изомерия возникает из-за различной последовательности связей между атомами углерода.
Таким образом, изомерия циклоалканов является важной характеристикой этих соединений, которая имеет прямое влияние на их свойства и реакции.
Номенклатура циклоалканов: правила и примеры
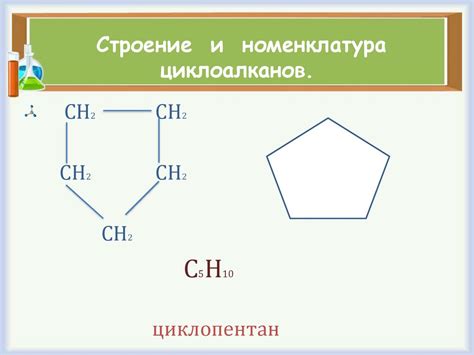
Циклоалканы - это насыщенные углеводороды, содержащие в своей структуре кольцевой углеродный фрейм. В них присутствуют только одинарные связи между атомами углерода. Номенклатура циклоалканов основана на принципе назначения префиксов в зависимости от числа атомов углерода, образующих кольцо.
Основные правила номенклатуры циклоалканов:
- Определить число атомов углерода в кольце. Это число указывается в качестве префикса перед названием углеводорода.
- Использовать префиксы ene или yne для указания двойной или тройной связи, соответственно. В циклоалканах применение этих префиксов недопустимо, так как в кольце отсутствуют двойные и тройные связи.
- Если в кольце присутствуют одинаковые радикалы, их должно быть указано соответствующее число перед названием углеводорода.
Примеры названий циклоалканов:
| Число атомов углерода | Название |
|---|---|
| 3 | циклопропан |
| 4 | циклобутан |
| 5 | циклопентан |
| 6 | циклогексан |
В случае, если в кольце присутствуют различные радикалы, их можно указывать в алфавитном порядке или в порядке их появления в молекуле.
Например:
- циклопентан - если кольцо состоит только из одинаковых атомов углерода;
- трилиза - если имеется один радикал;
- циклопентил - если имеется один радикал;
- 3-метилциклобутан - если в кольце присутствуют два одинаковых атома углерода и один метильный радикал.
Таким образом, номенклатура циклоалканов представляет собой набор правил, позволяющих определить и назвать циклические углеводороды в зависимости от их структуры и числа атомов углерода в кольце.
Электронное строение и виды напряжений в циклоалканах

Циклоалканы - это ациклические углеводороды, молекулы которых образуют замкнутые алкановые структуры. Однако, в отличие от алканов, циклоалканы обладают определенными особенностями в своем электронном строении, которые связаны с особенностями замкнутой структуры молекулы.
Все атомы углерода в циклоалканах образуют сп3-гибридизованные орбитали, что обеспечивает им химическую стабильность. Однако, из-за замкнутой структуры могут возникать определенные электронные эффекты, которые приводят к нарушению идеальной геометрии молекулы и возникновению напряжений.
Виды напряжений в циклоалканах можно разделить на две основные категории:
- Угловое напряжение: возникает из-за угломерного отклонения атомов углерода от идеального значению для энергетических побуждений, что приводит к возникновению напряжений в молекуле.
- Линейное напряжение: возникает из-за отклонения связей углерод-углерод от идеальной длины. Линейное напряжение связано с тем, что замкнутая структура циклоалканов не может идеально вытянуться в прямую линию без значительного энергетического затрат.
Угловое и линейное напряжения могут влиять на реакционную способность циклоалканов и порядок реакций, в которых они участвуют. Напряжения могут вызывать реакции, такие как открытие кольцевых структур, а также могут влиять на образование продуктов реакции.
| Количество атомов углерода в кольце | Напряжение (кДж/моль) |
|---|---|
| 3 | 27.5 |
| 4 | 18.2 |
| 5 | 8.6 |
| 6 | 0 |
| 7 | 7.1 |
| 8 | 19.8 |
| 9 | 31.9 |
Таким образом, виды напряжений в циклоалканах зависят от их электронного строения и наличия многочисленных сп3-гибридизованных атомов углерода в замкнутой структуре. Угловое и линейное напряжения могут быть значительными и влиять на реакционную способность молекулы, что делает их интересными объектами для исследований в органической химии.
Вопрос-ответ

Что такое циклоалканы?
Циклоалканы - это класс органических соединений, состоящих из углеродных атомов, образующих замкнутую кольцевую структуру. У них отсутствует двойная или тройная связь между атомами углерода.
Как классифицируются циклоалканы?
Циклоалканы могут быть классифицированы по количеству атомов углерода в кольце. Например, циклогексан - шестичленное кольцо, циклопентан - пятичленное кольцо и т.д.
Что такое изомерия у циклоалканов?
Изомерия - это явление, когда у соединений одинаковая молекулярная формула, но различное химическое или структурное строение. У циклоалканов существуют два типа изомерии: маслянистая (конформационная) и структурная (циклическая).
Какая номенклатура используется для называния циклоалканов?
Для называния циклоалканов используется система номенклатуры Менделеева-Преображенского. Каждый легкий циклоалкан имеет префикс "цикло-", за которым следует числительное, обозначающее количество атомов углерода. Например, циклопентан, циклогексан и т.д.
Какие виды напряжений могут быть у циклоалканов?
Циклоалканы имеют свойство накопления энергии в связях, когда атомы углерода оказываются на слишком малом расстоянии друг от друга. В результате возникают различные виды напряжений: угловые напряжения, напряжения этиленового типа и т.д.