Молекула натрия хлорида (NaCl) состоит из атомов натрия и хлора. Натрий и хлор являются элементами, принадлежащими к группе щелочных металлов и группе галогенов соответственно.
Молекула NaCl имеет ионную структуру, что означает, что натрий и хлор образуют ионы, притягивающиеся друг к другу электростатическими силами. В результате образуется кристаллическая решетка, в которой каждый атом натрия окружен шестью атомами хлора, а каждый атом хлора окружен шестью атомами натрия.
Таким образом, каждая молекула NaCl содержит один атом натрия и один атом хлора. Вместе они образуют структуру, известную как ионная связь, делая молекулу NaCl стабильной и неделимой.
Структура молекулы NaCl

Молекула NaCl представляет собой химическое соединение, состоящее из атомов натрия (Na) и хлора (Cl). Эти атомы образуют ионную связь, что обуславливает особую структуру молекулы.
В молекуле NaCl один атом натрия (Na) соединяется с одним атомом хлора (Cl) через ковалентную связь. При этом атом натрия отдает один электрон атому хлора, образуя положительный ион Na+ и отрицательный ион Cl-. Эти ионы притягиваются друг к другу электростатическими силами и образуют стабильную молекулу NaCl.
Структура молекулы NaCl можно представить в виде кристаллической решетки, в которой ионы натрия и хлора расположены в упорядоченном способе. Каждый ион натрия окружен шестью ионами хлора, а каждый ион хлора окружен шестью ионами натрия. Такая структура обеспечивает стабильность и прочность молекулы NaCl.
В молекуле NaCl содержится ровно один атом натрия (Na) и один атом хлора (Cl), что означает, что общее количество атомов в молекуле равно двум. Такая простая структура делает молекулу NaCl одним из самых распространенных и известных химических соединений.
Химическая формула и вещественный состав
Химическая формула - это символьное обозначение, содержащее информацию о количестве и типе атомов, входящих в молекулу вещества. Она позволяет описать состав и структуру химического соединения. В химии символы элементов обычно обозначаются заглавными буквами, а индексы, указывающие на количество атомов каждого элемента, пишутся справа от символов.
Вещественный состав - это представление о том, из каких элементов состоит данное вещество и в каких пропорциях они присутствуют. В случае с хлоридом натрия (NaCl) вещественный состав указывает, что молекула содержит атом натрия (Na) и атом хлора (Cl) в пропорции 1:1.
Молекула NaCl состоит из одного атома натрия и одного атома хлора. Натрий относится к группе щелочных металлов и обладает одним атомом в своей молекуле, обозначаемым символом Na. Хлор является галогеном и также содержит один атом в своей молекуле, обозначаемый символом Cl. При соединении этих двух элементов образуется одна молекула NaCl, в которой атомы натрия и хлора связаны ионной связью.
Химическая формула NaCl является простейшей ионной формулой, которая отображает то, что в грамме NaCl содержится число атомов натрия и хлора, соответствующее их молярной массе. Таким образом, массовая доля натрия в молекуле NaCl составляет 22,99%, а массовая доля хлора равна 77,01%.
Молекулярная масса и атомы

Молекулярная масса является одним из важных характеристик химического вещества и определяется суммой атомных масс всех атомов, входящих в его молекулу. Молекулярная масса позволяет узнать, сколько атомов содержится в молекуле данного вещества.
Атом является основной единицей химической структуры вещества, и его масса измеряется в атомных единицах (а.е.м.). Атомы соединяются между собой, образуя молекулу, которая может состоять из одного или нескольких разных атомов. Например, в молекуле воды (H2O) содержатся два атома водорода и один атом кислорода.
Для расчета молекулярной массы вещества необходимо знать атомные массы всех атомов, входящих в его молекулу. Эти значения указаны в периодической системе химических элементов. Например, атомная масса натрия (Na) равна примерно 22,99 а.е.м., а атомная масса хлора (Cl) составляет приблизительно 35,45 а.е.м.
Молекулярная масса вещества рассчитывается путем сложения атомных масс всех его атомов. В случае молекулы натрия хлорида (NaCl) масса натрия составляет примерно 22,99 а.е.м., а масса хлора - около 35,45 а.е.м. Следовательно, молекулярная масса NaCl равна примерно 58,44 а.е.м.
Таким образом, в молекуле натрия хлорида (NaCl) содержится один атом натрия и один атом хлора. Эти атомы соединяются между собой, образуя кристаллическую решетку, и обладают определенными химическими и физическими свойствами, характерными для данного соединения.
Структура кристаллической решетки
Кристаллическая решетка представляет собой пространственную структуру, образованную атомами или ионами, которые располагаются в определенном порядке. Это порядочное расположение атомов или ионов обусловлено их взаимодействием и создает особые свойства кристаллических веществ.
Структура кристаллической решетки NaCl относится к типу ионной связи. В данной структуре натрий (Na) является катионом, обладающим положительным зарядом, а хлор (Cl) - анионом с отрицательным зарядом. Каждый натрийный ион окружен шестью хлоровыми ионами, а каждый хлоровый ион окружен шестью натриевыми ионами.
Молекула NaCl состоит из одного атома натрия и одного атома хлора. В кристаллической решетке NaCl эти молекулы образуют регулярную трехмерную структуру, где каждый ион окружен другими ионами, и силы электростатического притяжения поддерживают их на своих местах.
В итоге, в молекуле NaCl содержится один атом натрия и один атом хлора. Общее количество атомов в молекуле NaCl равно двум.
Ионные связи и электроотталкивание
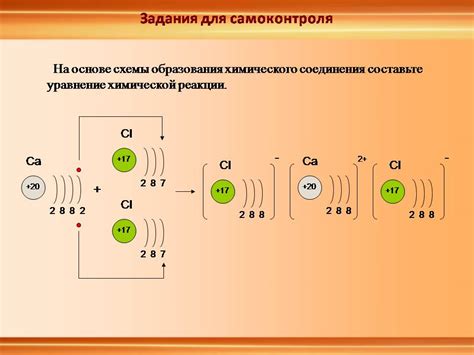
Ионная связь - это особый тип химической связи, который образуется между атомами, когда один атом отдает электрон(ы), становясь положительным ионом (катионом), а другой атом принимает эти электроны, становясь отрицательным ионом (анионом). Сильную связь в ионной связи обеспечивает силы электростатического притяжения между положительно и отрицательно заряженными ионами.
Электроотталкивание - это явление, которое возникает, когда два отрицательно заряженных атома или молекулы приближаются друг к другу. В данном случае, отрицательные электрические заряды отталкиваются и возникает отталкивающая сила. В силу принципа сохранения заряда, атомы и молекулы будут стремиться избегать слишком близкого контакта, чтобы избежать отталкивающих сил.
Когда молекула NaCl образуется, натрий (Na) отдает один электрон, становясь положительно заряженным натриевым ионом (Na+), а хлор (Cl) принимает этот электрон, становясь отрицательно заряженным хлоридным ионом (Cl-). В результате образуется ионная связь между Na+ и Cl-, обеспечивающая стабильность молекулы NaCl. В данном случае, силы электростатического притяжения между положительно и отрицательно заряженными ионами перевешивают отталкивающие силы.
Молекула NaCl содержит один натриевый ион (Na+) и один хлоридный ион (Cl-), то есть общее количество атомов равно двум. Ионная связь в молекуле NaCl обладает сильной прочностью и хорошей стабильностью, что делает NaCl одним из наиболее известных ионных соединений.
Координационное число
Координационное число в химии отражает число ближайших соседей, окружающих атом или ион в кристаллической структуре вещества. Оно указывает на количество атомов или ионов, с которыми данный атом или ион связано непосредственно. Координационное число имеет важное значение для определения физических и химических свойств вещества.
Например, в кристаллической структуре хлорида натрия (NaCl) координационное число натриевого и хлорного атомов равно 6. Это означает, что каждый натриевый и хлорный атом имеет шесть ближайших соседей, с которыми непосредственно связаны.
Координационное число может быть различным для разных типов атомов или ионов в веществе. Оно зависит от типа кристаллической решетки и взаимного расположения атомов или ионов в ней. Например, в кристаллической структуре алмаза координационное число каждого углеродного атома составляет 4, так как он связан с четырьмя ближайшими соседями в форме тетраэдра.
Координационное число имеет важное значение в различных областях химии и материаловедения. Оно позволяет предсказать и объяснить различные свойства веществ, такие как термохимическая стабильность, кристаллическая структура, магнитные и электрические свойства и т. д. Таким образом, изучение координационного числа является важной составляющей химического анализа и исследования веществ.
Симметрия решетки и структурные узлы
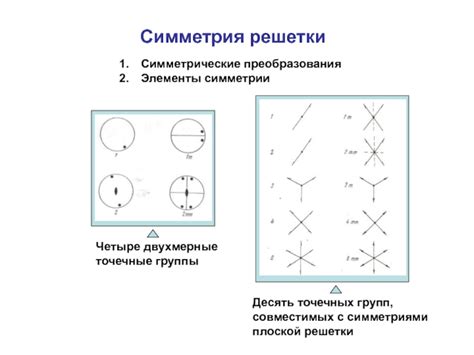
Симметрия решетки является одной из ключевых характеристик кристаллических веществ. Решетка - это трехмерная узорная структура, которая состоит из одинаковых структурных узлов, повторяющихся в пространстве. Симметрия решетки определяет, какие преобразования или операции можно применять к решетке, не изменяя ее внешнего вида.
Существует несколько типов симметрии решетки, таких как осевая симметрия, плоскостная симметрия и центральная симметрия. Осевая симметрия означает, что решетка выглядит одинаково при повороте на определенный угол. Плоскостная симметрия означает, что решетка выглядит одинаково при зеркальном отражении относительно плоскости. Центральная симметрия означает, что решетка выглядит одинаково при повороте на 180 градусов относительно центра.
Структурные узлы - это атомы или группы атомов, которые занимают определенные позиции в решетке. Каждый структурный узел представляет собой точку в трехмерном пространстве, где находится атом. Структурные узлы могут быть одномерными, двумерными или трехмерными в зависимости от сложности решетки.
Атомы в молекуле NaCl состоят из натрия (Na) и хлора (Cl). Решетка NaCl имеет кубическую симметрию и состоит из атомов натрия, которые занимают узлы кубической решетки, и атомов хлора, которые занимают узлы, сдвинутые относительно кубической решетки. Таким образом, в молекуле NaCl содержится один атом натрия и один атом хлора.
Содержание атомов в молекуле NaCl
Молекула обычной кухонной соли, натрия хлорида (NaCl), состоит из атомов натрия и атомов хлора, связанных в ионную решетку. Натрий является щелочным металлом, а хлор - неметаллом.
В молекуле NaCl содержится один атом натрия (Na) и один атом хлора (Cl). Эти атомы объединены в ионную связь, где натрий отдаёт один электрон хлору. При этом натрий становится положительным ионом (Na+) с одной внешней электронной оболочкой, а хлор - отрицательным ионом (Cl-) с полной внешней электронной оболочкой.
В результате такой связи одна молекула NaCl содержит один атом натрия (Na) и один атом хлора (Cl), образуя кристаллическую структуру соли. Такая связь и образование ионной решетки являются характерными свойствами соединения NaCl и отличают его от координационных связей, которые наблюдаются в других молекулах.
Свойства и применение NaCl
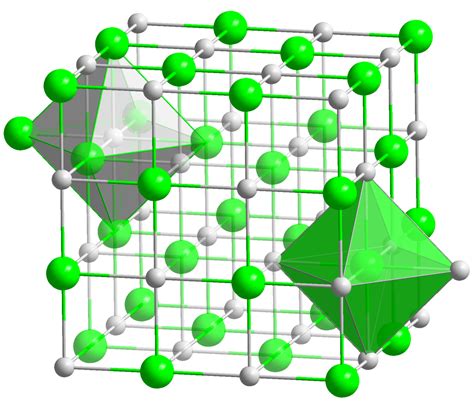
NaCl, или хлорид натрия, является важным химическим веществом, которое широко используется в различных областях.
Физические свойства:
- NaCl представляет собой белый кристаллический порошок или кристаллы в виде кубических или икосаэдрических сверток.
- Он обладает высокой теплостойкостью и плавится при температуре около 800°C.
- NaCl легко растворяется в воде и многих других растворителях, что делает его доступным для использования в различных процессах.
Химические свойства:
- NaCl обладает высокой стабильностью и химической инертностью.
- Он не проявляет реактивности с большинством веществ, за исключением некоторых сильных окислителей или редких элементов.
- NaCl может образовывать растворы с различными концентрациями, от слабых до насыщенных, что позволяет использовать его для регулирования вязкости и электролитного баланса.
Применение:
- NaCl применяется в пищевой промышленности в качестве консерванта и приправы к пище.
- Он используется в химической промышленности для производства различных химических соединений.
- NaCl также широко применяется в медицине для оральной регидратации при обезвоживании и во время некоторых медицинских процедур.
- Он используется в производстве стекла, водопроводных систем и других промышленных материалов.
В целом, NaCl является важным химическим соединением, которое находит широкое применение в различных отраслях и областях, благодаря своим уникальным свойствам и химической стабильности.
Вопрос-ответ
Какое количество атомов содержится в молекуле NaCl?
Молекула NaCl, или хлорида натрия, не является молекулой в привычном понимании. Она образуется при образовании ионной связи между атомами натрия (Na) и хлора (Cl). При этом образуется кристаллическая решетка, в которой каждый ион натрия окружен шестью ионами хлора, а каждый ион хлора окружен шестью ионами натрия. Таким образом, в каждой единице кристаллической решетки NaCl содержится по одному атому натрия и хлора.
Сколько атомов натрия и хлора содержится в молекуле NaCl?
Молекула NaCl не содержит атомов в привычном понимании. Натрий (Na) и хлор (Cl) образуют ионные решетки, где каждому атому натрия соответствует атом хлора и наоборот. Таким образом, в каждой единице кристаллической решетки NaCl содержится по одному атому натрия и хлора.
Я знаю, что молекула NaCl образуется из атомов натрия и хлора. Сколько атомов содержится в одной молекуле NaCl?
Молекула NaCl не образуется из атомов натрия и хлора в привычном понимании. Натрий (Na) и хлор (Cl) образуют ионные решетки, где каждому атому натрия соответствует атом хлора и наоборот. Таким образом, в каждой единице кристаллической решетки NaCl содержится по одному атому натрия и хлора.
Какие атомы входят в состав молекулы NaCl?
Молекула NaCl не состоит из атомов в привычном понимании. Она образуется при образовании ионной связи между атомами натрия (Na) и хлора (Cl). Таким образом, в состав молекулы NaCl входят атом натрия и атом хлора.
Какой химический элемент входит в состав молекулы NaCl?
В состав молекулы NaCl входят химические элементы: натрий (Na) и хлор (Cl).
Почему молекула NaCl не содержит больше одного атома?
Молекула NaCl формируется при образовании ионной связи между атомами натрия (Na) и хлора (Cl), в результате которой образуется кристаллическая решетка. В каждой единице кристаллической решетки NaCl содержится по одному атому натрия и хлора.