Реакции кислорода с металлами являются очень важными химическими процессами, которые происходят в различных условиях. Кислород, будучи высокоэлектроотрицательным элементом, проявляет свою активность при взаимодействии с металлами. От этой реакции зависят различные физические и химические свойства материалов, которые используются в различных отраслях промышленности и научных исследованиях.
Во время реакции кислорода с металлами обычно происходит окисление металла. Кислород вступает в химическое соединение с металлом, формируя оксид. Степень окисления металла в оксиде определяет его физические и химические свойства. Некоторые металлы образуют множество оксидов с разной степенью окисления, что отражается на их цвете, плотности, пластичности и других свойствах.
Уравнения реакций кислорода с металлами могут быть простыми или сложными, в зависимости от конкретной реакции и условий, в которых она происходит. Важно точно определить стехиометрические коэффициенты в уравнении, чтобы соблюсти закон сохранения массы. Также необходимо учитывать физические и химические свойства металла, такие как его активность, степень окисления и способность к образованию соединений с кислородом.
Изучение реакций кислорода с металлами является важной задачей современной химии. Оно позволяет не только лучше понять основы химической реактивности металлов, но и разрабатывать новые материалы с определенными свойствами. Различные оксиды, полученные в результате реакций кислорода с металлами, широко применяются в промышленности, в том числе в производстве красок, пластмасс, керамики и других материалов.
Реакции кислорода с металлами: основные моменты
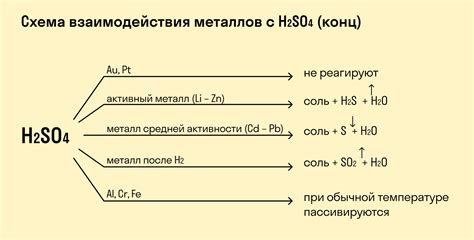
Реакции кислорода с металлами являются одним из основных процессов в химии. Кислород имеет высокую электроотрицательность и способен образовывать связи с металлическими элементами. Реакция кислорода с металлами происходит в результате окисления металла, при котором кислород принимает электроны от металла.
Уравнения реакций кислорода с металлами можно представить в виде химических формул. Например, реакция кислорода с железом может быть представлена уравнением: Fe + O2 → FeO. В этой реакции железо окисляется, а кислород восстанавливается.
Также существуют реакции кислорода с металлами, при которых образуются оксиды. Например, реакция кислорода с алюминием может быть представлена уравнением: 4Al + 3O2 → 2Al2O3. В этой реакции алюминий окисляется до оксида алюминия, который образует защитную пленку на поверхности металла.
Реакции кислорода с металлами могут иметь различные скорости и условия протекания. Например, при нагревании реакции протекают быстрее, чем при комнатной температуре. Также на скорость реакции может влиять поверхность металла и наличие катализаторов.
Изучение реакций кислорода с металлами имеет большое практическое значение. Многие металлы используются в различных отраслях промышленности и их взаимодействие с кислородом может привести к коррозии и разрушению конструкций. Поэтому важно знать основные моменты этих реакций для правильного выбора и применения металлических материалов.
Примеры реакций металлов с кислородом в среде воздуха
Воздух содержит около 20% кислорода, и многие металлы способны реагировать с ним, образуя оксиды. Реакции кислорода с металлами происходят в результате окисления металла, когда он отдает электроны.
Простейшим примером реакции металла с кислородом в среде воздуха является горение. Например, при нагревании магния он реагирует с кислородом, выделяя яркий белый свет и образуя оксид магния (MgO).
Еще один пример реакции – ржавление железа. Когда железо находится на воздухе, оно вступает в реакцию с кислородом и образует оксид железа (Fe2O3), который обычно называют ржавчиной. Этот процесс непрерывно протекает на поверхности металла и приводит к его разрушению.
Некоторые металлы, такие как алюминий и цинк, также реагируют с кислородом воздуха, но формируют защитную пленку оксидов на своей поверхности. Эта пленка защищает металл от дальнейшего окисления и называется "пассивной".
Факторы, влияющие на скорость реакций кислорода с металлами

1. Величина поверхности металла. Чем больше площадь поверхности металла, тем больше активных участков доступно для взаимодействия с молекулами кислорода. Поэтому частицы металла в виде порошка или мелких частиц значительно быстрее реагируют с кислородом по сравнению с металлическими блоками большого размера.
2. Концентрация кислорода. Высокая концентрация кислорода в окружающей среде позволяет большему количеству молекул вступить в реакцию с металлом за единицу времени, что ускоряет процесс окисления. Например, в присутствии кислорода воздуха процесс окисления металла будет происходить быстрее, чем в инертной газовой среде.
3. Температура. Повышение температуры обычно увеличивает скорость химических реакций, в том числе и реакций металлов с кислородом. Высокая температура обеспечивает молекулам большую кинетическую энергию, что способствует их более активному движению и столкновениям, ускоряя тем самым реакцию окисления металла.
4. Вид металла. Различные металлы обладают разными скоростями окисления под воздействием кислорода. Например, активные щелочные металлы, такие как натрий и калий, сильно реагируют с кислородом, образуя оксиды, в то время как некоторые металлы, например, золото, платина и серебро, кислородом почти не реагируют.
5. Наличие катализаторов. Некоторые вещества могут ускорять реакцию окисления металла, действуя как катализаторы. Катализаторы способствуют снижению энергии активации и ускоряют процесс реакции без изменения своей структуры. Например, напыление металлов на поверхности пористого катализатора может значительно увеличить скорость и эффективность окисления металлов.
6. Взаимодействие с другими веществами. Наличие других веществ, таких как вода или кислоты, может существенно изменить скорость реакции металла с кислородом. Например, металлы могут быстро реагировать с водой, образуя оксиды и водород, что ускоряет процесс окисления. Также наличие некоторых кислот может способствовать образованию короткого оксидного слоя на поверхности металла, что ускоряет реакцию с кислородом.
Значение реакций кислорода с металлами в повседневной жизни
Реакции кислорода с металлами играют важную роль в повседневной жизни человека. Одним из самых популярных примеров такой реакции является окисление железа, что приводит к образованию ржавчины. Ржавчина может повредить поверхность металлических предметов, делая их менее привлекательными и ухудшая их функциональность.
Еще один важный пример реакции кислорода с металлами - образование оксидов. Когда металл вступает в контакт с кислородом, образуются соединения, называемые оксидами. Эти оксиды могут иметь разные свойства и использоваться в различных отраслях промышленности и производстве. Например, оксид алюминия используется в производстве алюминиевых сплавов и керамики, а оксид меди - в производстве электронных компонентов.
Кроме того, реакции кислорода с металлами применяются в химическом анализе. Например, при определении содержания кислорода в составе материала, происходит его взаимодействие с металлами, что позволяет определить количество находящегося в веществе кислорода.
Вопрос-ответ
Что такое реакции кислорода с металлами?
Реакции кислорода с металлами — это химические реакции, при которых кислород соединяется с металлом, образуя оксид металла. В результате таких реакций металлы окисляются.
Какие уравнения реакций кислорода с металлами существуют?
Уравнения реакций кислорода с металлами могут быть различными, в зависимости от металла и условий реакции. Однако общая формула таких уравнений выглядит следующим образом: металл + кислород → оксид металла. Например, уравнение реакции кислорода с алюминием выглядит так: 4 Al + 3 O2 → 2 Al2 O3.
Какие металлы реагируют с кислородом?
Почти все металлы могут реагировать с кислородом. Некоторые металлы, такие как железо и алюминий, способны реагировать с кислородом при комнатной температуре. Другие металлы, такие как магний или кальций, могут реагировать только при нагревании. Однако есть и такие металлы, которые не реагируют с кислородом, например, золото или платина.
Чему соответствует оксид металла в уравнении реакции кислорода с металлами?
Оксид металла, образующийся в результате реакции кислорода с металлами, можно рассматривать как соединение кислорода и металла. Оксид металла является результатом окисления металла кислородом. Например, в уравнении реакции кислорода с железом образуется оксид железа (III) - Fe2 O3.
В чем заключается значимость реакций кислорода с металлами?
Реакции кислорода с металлами имеют большое значение в химии и промышленности. Например, окисление металла позволяет получать оксиды, которые имеют широкое применение в качестве катализаторов, керамики, стекла и т.д. Кроме того, реакции кислорода с металлами играют важную роль в процессах коррозии металлов, которые необходимо учитывать при эксплуатации металлических конструкций.