Атомы металлов являются основными строительными блоками вещества, обладающего металлическими свойствами. Как правило, такие атомы имеют сложную электронную структуру, включающую несколько оболочек электронов. Однако, особенностью атомов металлов является то, что их внешняя оболочка содержит от 1 до 3 электронов.
Электроны находятся в орбиталях, или энергетических уровнях, вокруг ядра атома. Внешняя оболочка, или последняя заполненная энергетическая оболочка, определяет химические свойства атома. У атомов металлов внешняя оболочка состоит из s- и p-орбиталей, которые могут вмещать от 1 до 3 электронов.
Это свойство атомов металлов имеет важное значение для их химической активности. Внешние электроны обладают свободными энергетическими уровнями и могут легко участвовать в химических реакциях. Количество электронов во внешней оболочке определяет, как металл будет взаимодействовать с другими атомами и веществами.
Таким образом, внешняя оболочка атомов металлов, содержащая 1-3 электрона, играет ключевую роль в их химических свойствах и взаимодействии с окружающей средой. Понимание этого факта является важным для исследования и применения металлических материалов в различных областях науки и промышленности.
Внешняя оболочка атомов металлов
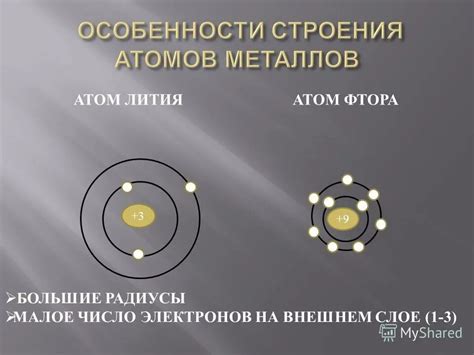
Внешняя оболочка атомов металлов играет важную роль в их химических и физических свойствах. Оболочка, или внешний электронный слой, состоит из электронов, находящихся на самом высоком энергетическом уровне в атоме.
У большинства атомов металлов внешняя оболочка содержит от одного до трех электронов. Эти электроны называются валентными, поскольку они определяют химические свойства атома.
Благодаря наличию валентных электронов, металлы обладают характерными свойствами, такими как хорошая электропроводность, гибкость и теплопроводность. Валентные электроны образуют свободные электронные облака, которые способны перемещаться в кристаллической решетке металла, обеспечивая его электропроводность.
Кроме того, внешняя оболочка металлических атомов определяет их способность образовывать химические связи с другими атомами. Металлы обычно образуют ионные связи с неметаллами, отдавая валентные электроны и приобретая положительный заряд. Это позволяет им образовывать стабильные соединения и обладать высокой реакционной способностью.
Из чего состоит внешняя оболочка атомов металлов
Внешняя оболочка атомов металлов состоит из электронов, которые находятся на самом внешнем энергетическом уровне. Обычно внешняя оболочка содержит 1-3 электрона.
Внешняя оболочка атомов металлов играет важную роль в химических реакциях и свойствах металлов. Эти электроны называются валентными электронами и отвечают за химическую активность металла.
Количество валентных электронов в внешней оболочке атомов металлов определяет их способность образовывать химические связи с другими атомами. Чем больше валентных электронов у атома металла, тем больше возможностей у него для образования связей соединений и тем большую химическую активность он проявляет.
Соединения металлов с другими элементами и атомами обычно основаны на обмене или передаче валентных электронов. Взаимодействие этих электронов позволяет металлам образовывать ионы, молекулы и сложные соединения.
Знание количества валентных электронов и их расположения в внешней оболочке атомов металлов помогает понять, как металлы взаимодействуют с другими веществами и почему они обладают определенными химическими и физическими свойствами.
Сколько электронов содержит внешняя оболочка атомов металлов

Внешняя оболочка атомов металлов может содержать от одного до трех электронов. Количество электронов во внешней оболочке влияет на химические свойства и реактивность металлов.
Одним из основных свойств металлов является способность отдавать электроны из внешней оболочки. Если внешняя оболочка содержит всего один электрон, металл будет обладать высокой активностью, поскольку его легко отдать. Это делает металлы с одним электроном на внешней оболочке отличными проводниками электричества и тепла.
Металлы с двумя электронами на внешней оболочке также обладают хорошей проводимостью, но их реактивность не так высока, как у металлов с одним электроном. Однако, металлы с двумя электронами на внешней оболочке могут образовывать различные соединения и обладать разнообразными свойствами.
Некоторые металлы имеют три электрона на внешней оболочке. Это делает их менее реактивными, чем металлы с одним или двумя электронами. Такие металлы обычно образуют стабильные соединения и часто используются в промышленности и технологиях.
Влияние количества электронов на свойства металлов
Внешняя оболочка атомов металлов содержит 1-3 электрона. Количество электронов во внешней оболочке крайне важно для свойств металлов и их химической активности. У металлов, у которых внешняя оболочка содержит только один электрон, наблюдается высокая химическая активность и хорошая проводимость электричества.
Такие металлы, например, натрий и калий, легко реагируют с водой и кислородом. Они обладают низким плавлением и кипением. Одноэлектронные элементы металлов также обладают хорошими механическими свойствами, что делает их подходящими для использования в различных промышленных отраслях.
У металлов с двумя электронами во внешней оболочке также высокая химическая активность, однако эта активность немного ниже, чем у одноэлектронных металлов. Эти металлы обладают некоторыми характеристиками, подобными свойствам одноэлектронных металлов, но частично проявляют и свойства металлов с тремя электронами во внешней оболочке.
Металлы, у которых во внешней оболочке содержится три электрона, обладают достаточно низкой химической активностью. Это позволяет им быть стабильными и не очень реактивными. Такие металлы, как железо и алюминий, широко используются в различных промышленных целях, включая строительство, автомобильную промышленность и электронику. Они обладают хорошими магнитными и механическими свойствами, а также высокой прочностью.
Основные свойства металлов с 1 электроном во внешней оболочке

Металлы с одним электроном во внешней оболочке обладают рядом уникальных свойств, которые делают их важными элементами в различных областях науки и техники.
Во-первых, эти металлы обладают высокой электропроводностью. Это связано с тем, что один электрон в внешней оболочке может свободно перемещаться между атомами, создавая электрический ток. Эта свойство делает эти металлы идеальными для использования в проводниках и различных электронных устройствах.
Во-вторых, металлы с одним электроном во внешней оболочке обладают высокой теплопроводностью. Это означает, что они способны быстро и равномерно передавать тепло. Благодаря этому свойству такие металлы широко применяются в конструкциях, требующих эффективного отвода тепла, например, в системах охлаждения электроники.
Еще одно важное свойство данных металлов - их способность образовывать стабильные и прочные связи с другими атомами. Это делает их основными строительными элементами в многих материалах, таких как металлические сплавы и каркасы конструкций.
Еще одним замечательным свойством металлов с одним электроном является их высокая реактивность. Они легко взаимодействуют с другими элементами, образуя химические соединения и реагируя с окружающей средой. Благодаря этому свойству такие металлы активно используются в различных химических реакциях и процессах.
Основные свойства металлов с 2 электронами во внешней оболочке
Металлы, у которых во внешней оболочке содержится два электрона, обладают рядом уникальных свойств, которые определяют их поведение и химическую активность.
Во-первых, два электрона во внешней оболочке металлов способствуют образованию металлической связи. Это означает, что электроны свободно передвигаются по кристаллической решетке металла, создавая электронное облако. Благодаря этому, металлы характеризуются высокой электропроводностью и теплопроводностью.
Во-вторых, именно наличие двух электронов во внешней оболочке металлов позволяет им образовывать химические связи с другими атомами. Это происходит путем отдачи этих электронов, что приводит к образованию ионов с положительным зарядом - катионов. Таким образом, металлы с двумя электронами во внешней оболочке проявляют металлическую химическую активность и способность образовывать ионные соединения.
Кроме того, металлы с двумя электронами во внешней оболочке отличаются высокой пластичностью и текучестью. Это обусловлено наличием свободных электронов, которые обеспечивают металлам возможность претерпевать деформации при воздействии давления или теплового воздействия без разрушения их структуры.
Таким образом, металлы с двумя электронами во внешней оболочке обладают рядом уникальных свойств, включая хорошую электропроводность, способность к образованию ионных соединений и высокую пластичность.
Основные свойства металлов с 3 электронами во внешней оболочке

Металлы с 3 электронами во внешней оболочке обладают рядом уникальных свойств, которые определяют их химическую активность и широкое применение в различных отраслях промышленности.
Во-первых, металлы с 3 электронами во внешней оболочке обладают высокой электропроводностью. Это связано с тем, что эти электроны легко двигаются по металлической решетке, образуя так называемую "электронную газ". Именно она обеспечивает возможность передачи электрического тока через металлы с минимальными потерями.
Во-вторых, металлы с 3 электронами во внешней оболочке имеют высокую теплопроводность. Это свойство позволяет им эффективно передавать тепло в процессе теплообмена. Благодаря этому металлы применяются в технике и строительстве для создания элементов, работающих при высоких температурах.
Кроме того, металлы с 3 электронами во внешней оболочке обладают высокой пластичностью и прочностью. Это свойство позволяет им легко подвергаться деформации без разрушения, что делает их удобными для формовки и создания различных конструкций.
И наконец, металлы с 3 электронами во внешней оболочке обладают химической активностью. Они способны легко образовывать соединения с другими элементами, особенно с неметаллами. Благодаря этому свойству металлы используются в химической промышленности для получения различных полезных веществ.
Итак, металлы с 3 электронами во внешней оболочке сочетают в себе такие важные свойства, как высокая электропроводность, теплопроводность, пластичность, прочность и химическая активность. Благодаря этим свойствам они широко применяются в различных отраслях промышленности и находят применение в производстве электроники, строительстве, автомобильной промышленности и других сферах жизни человека.
Вопрос-ответ
Зачем металлам нужны электроны во внешней оболочке?
Электроны во внешней оболочке металлов играют ключевую роль в химических реакциях и влияют на их физические и электрические свойства. Они также определяют способность металлов проводить электричество и тепло.
Почему внешняя оболочка атомов металлов содержит только 1-3 электрона?
Это связано с особенностями электронной структуры металлов. Металлы находятся в левой части периодической системы элементов и имеют малое число электронов в своей внешней оболочке. Об этом свидетельствует их химическая активность и способность образовывать ионные связи.
Как электроны во внешней оболочке металлов влияют на их свойства?
Электроны во внешней оболочке металлов определяют их способность проводить электричество и тепло. Большинство металлов обладают хорошей электропроводностью, так как электроны в их внешней оболочке могут свободно перемещаться под воздействием электрического поля. Они также влияют на другие физические свойства металлов, такие как пластичность и оптическая отражательность.
Может ли внешняя оболочка атомов металлов содержать более 3 электронов?
Да, внешняя оболочка атомов металлов может содержать более 3 электронов. Однако большинство металлов имеют 1-3 электрона в своей внешней оболочке, что делает их особенно активными химическими элементами.
Какие металлы имеют 1-3 электрона во внешней оболочке?
Металлы в общем случае могут содержать от 1 до 3 электронов в своей внешней оболочке. Некоторые примеры металлов с 1 электроном во внешней оболочке включают литий, натрий и калий. Примеры металлов с 2 электронами во внешней оболочке включают магний, кальций и стронций. Металлы с 3 электронами во внешней оболочке включают бор, алюминий и галлий.
