Химический элемент хлор (Cl) является одним из наиболее известных и распространенных элементов в природе. Он был открыт в 1774 году и имеет атомный номер 17 в периодической таблице. По своим свойствам хлор является галогеном, то есть элементом VIII группы периодической таблицы.
Хлор характеризуется как неметалл, так как обладает одним из основных признаков неметаллов - низкой электропроводностью. Неметаллами обычно являются хабаровская тройка, инертгазы, а также легкие, неглубокие компоненты кислород-потуга. Чистый хлор представляет собой зеленовато-желтый газ с характерным запахом, который является сильным раздражителем для глаз и дыхательных путей.
Самым известным соединением хлора является хлорид натрия (NaCl), наиболее широко распространенная соль в мировых океанах и основной компонент столовой соли. Но наиболее интересное и важное соединение хлора - это его высший оксид - оксид хлора (Cl2O7). Формула этого соединения указывает, что хлор является металлом, так как оксидное число его атомов в этом соединении составляет +7.
Хлор: металл или неметалл?

Хлор – химический элемент с атомным номером 17 и символом Cl. Он относится к неметаллам и находится в 17-й группе периодической системы элементов. Хлор обладает характерными свойствами неметалла, такими как низкая теплопроводность и электропроводность, хрупкость и низкая плотность.
В природе хлор встречается в виде солей, особенно хлоридов, которые широко распространены в морской воде, горных породах и почве. Хлор используется во многих отраслях промышленности, включая химическую, фармацевтическую и пищевую промышленность. Он также широко применяется в процессе очистки воды и в производстве пластиков и дезинфицирующих средств.
Формула высшего оксида хлора – Cl2O7. Это оксид кислоты хлорной, который образуется при взаимодействии хлора с кислородом. Клористый ангидрид используется в лабораторных условиях при получении других химических соединений и в процессе синтеза органических соединений.
Свойства хлора
1. Химическая активность: Хлор является одним из самых активных элементов в группе галогенов. Он обладает сильной окислительной способностью и может вступать в химические реакции с различными веществами.
2. Физические свойства: Хлор – газ желтовато-зеленого цвета с резким запахом. При комнатной температуре он легче воздуха и обладает высокой плотностью. Хлор может быть конденсирован при низких температурах и высоких давлениях.
3. Реакция с водой: Хлор обладает высокой растворимостью в воде. При контакте с водой образуется соляная кислота и образуется многоатомная отрицательная ион с хлором.
4. Реакция с металлами: Хлор реагирует с большинством металлов, образуя соли. Например, при взаимодействии с натрием образуется хлорид натрия.
5. Взаимодействие с органическими веществами: Хлор может реагировать с органическими веществами, образуя такие важные хлорированные органические соединения, как пластиковые полимеры, пестициды и лекарственные препараты.
6. Токсичность: Хлор является вредным веществом для организмов. При вдыхании его паров происходит раздражение слизистых оболочек дыхательных путей и глаз, а при попадании внутрь организма - отравление.
Хлор как неметалл

Хлор – один из известных неметаллов периодической системы элементов. Он относится к 17-ой группе, называемой галогены. Хлор обладает характерными свойствами неметаллов: он является малопроводящим электрический ток, неформирует ионы положительного заряда и образует ковалентные соединения.
Хлор обладает высокой электроотрицательностью, превышающей значение 3,0 по шкале Полинга. Это означает, что он имеет большую способность притягивать электроны к себе при образовании химических связей. Низкая проводимость электрического тока объясняется отсутствием свободных электронов в его кристаллической решетке.
Хлор образует множество ковалентных соединений с другими элементами. Его оксиды имеют формулу Cl2O, Cl2O2 и Cl2O6. При реакции с металлами хлор образует соли. Например, при взаимодействии с натрием получается хлорид натрия (NaCl) – широко используемая поваренная соль.
Таким образом, хлор является типичным неметаллом, обладающим характерными свойствами: неметаллы некондуктивны, образуют ковалентные соединения и имеют высокую электроотрицательность, что делает их агрессивными взаимодействующими веществами.
Хлор как металл
Хлор - один из химических элементов, принадлежащий к классу неметаллов, однако существует множество мнений о его классификации. В некоторых аспектах хлор может проявлять металлические свойства, что вызывает дискуссии среди ученых.
Металлоидный характер хлора проявляется в его способности образовывать положительные ионы, причем с энергией, сравнимой с некоторыми металлами. При этом хлорная кислота, которая содержит хлор, способна растворять многие металлы, а хлориды образуют цветные соединения с кобальтом и никелем.
Однако хлор все же классифицируется как неметалл, поскольку не обладает типичными металлическими свойствами. Хлор - газ при комнатной температуре и давлении, его молекулы образованы двумя атомами, и они обладают высокой электроотрицательностью. Кроме того, хлор не образует катионы и не обладает металлическим блеском.
Таким образом, хотя хлор в некоторых случаях может проявлять металлические свойства, на основании его общих характеристик он всё же относится к классу неметаллов.
Формула высшего оксида хлора
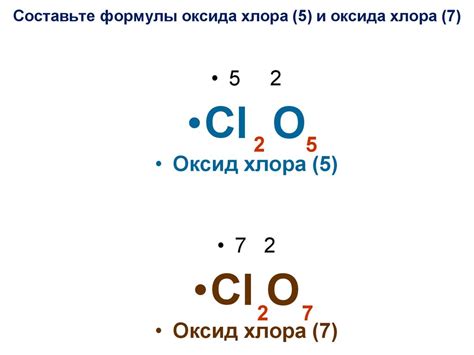
Высший оксид хлора имеет формулу Cl2O7 и представляет собой соединение хлора и кислорода. Такое соединение обладает сильной окислительной активностью и является аналогом высшего оксида серы (SO3).
Формула Cl2O7 означает, что в молекуле присутствуют две атомы хлора и семь атомов кислорода. Кислородные атомы образуют с хлором сильные ковалентные связи. При этом окислительное состояние хлора в данном соединении равно +7.
Высший оксид хлора является мощным окислителем и может взаимодействовать с различными веществами. Например, он способен окислять металлы, аммиак, сернистый ангидрид и другие соединения.
Формула Cl2O7 позволяет более точно описать состав и свойства высшего оксида хлора и сделать вывод о его окислительной активности.
Вопрос-ответ
Что такое хлор?
Хлор (Cl) - это химический элемент с атомным номером 17. Он принадлежит к группе галогенов и обладает отрицательным зарядом.
Является ли хлор металлом или неметаллом?
Хлор является неметаллом. Он отличается хрупкостью, низкой теплопроводностью и электропроводностью и обычно образует отрицательные ионы.
В каких формах присутствует хлор на Земле?
Хлор в свободном виде не существует на Земле из-за его реактивности. Он может быть найден в виде хлорида в различных минералах, таких как галит (хлорид натрия) и силвинит (хлорид калия).
Какова формула высшего оксида хлора?
Формула высшего оксида хлора известна как хлорат(V)."OCI" (хлорат(V)) имеет степень окисления хлора равную +5. Формула высшего оксида хлора описывает его химическую форму в соответствии с правилами назначения названия, где Cl обозначает атом хлора, а O обозначает атом кислорода.
Чем хлорат(V) отличается от других соединений хлора?
Хлорат(V) отличается от других соединений хлора тем, что в нем хлор имеет наибольшую степень окисления (+5), что делает его более окислительным и реакционноспособным. В отличие от других соединений хлора, таких как хлориды и гипохлориты, хлорат(V) чаще используется в качестве окислителя в различных химических реакциях.
Каковы основные свойства хлора?
Основные свойства хлора включают высокую реактивность, высокую электроотрицательность, хорошую растворимость в воде и других растворителях, а также способность к образованию кислотных оксидов. Он используется в различных отраслях промышленности, таких как производство пластиков, водоочистка и производство дезинфицирующих средств.
Какие другие соединения хлора известны?
Помимо хлората(V), другие известные соединения хлора включают хлориды (Cl-), такие как хлорид натрия (NaCl), гипохлориты (ClO-), такие как гипохлорит натрия (NaClO), а также множество органических соединений с присутствием атома хлора.

