Фосфаты - это соли, в которых фосфорная кислота (H3PO4) играет роль кислотного компонента, а металлы, такие как натрий (Na) и кальций (Ca), играют роль основного компонента. Фосфаты являются важными соединениями как в природе, так и в промышленности.
Фосфат натрия (Na3PO4) - это соль, образующаяся при реакции фосфорной кислоты с натрием. Он принадлежит к классу неорганических соединений и часто используется в пищевой и фармацевтической промышленности. Формула Na3PO4 указывает на то, что в каждой молекуле фосфата натрия содержатся три атома натрия.
Фосфат кальция (Ca3(PO4)2) - это соль, которая образуется при реакции фосфорной кислоты с кальцием. Фосфат кальция является основным компонентом костей и зубов человека и животных. Его также используют в производстве удобрений и при производстве строительных материалов. Формула Ca3(PO4)2 указывает на то, что в каждой молекуле фосфата кальция содержится три атома кальция и две молекулы фосфорной кислоты.
Фосфаты соединений металлов натрия и кальция: формулы и объяснение
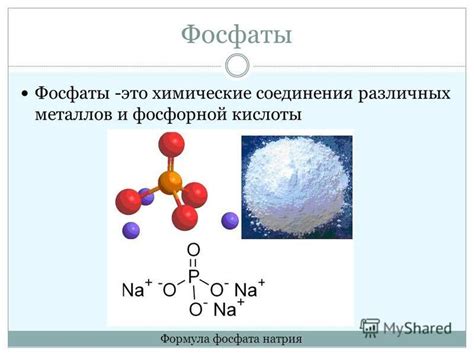
Фосфаты - это соединения фосфорной кислоты и металлов. Они играют важную роль в биологических системах и находят применение в различных отраслях промышленности. Рассмотрим формулы и некоторые свойства фосфатов соединений металлов натрия и кальция.
Формула фосфата натрия Na3PO4 состоит из ионов натрия (Na+) и иона фосфата (PO43-). В этом соединении каждый ион натрия будет иметь заряд +1, а каждый ион фосфата - заряд -3. Чтобы сбалансировать заряды и получить нейтральное соединение, необходимо 3 иона натрия для 1 иона фосфата. Таким образом, в формуле присутствует префикс "три" в обозначении натрия.
Формула фосфата кальция Ca3(PO4)2 содержит ионы кальция (Ca2+) и ионы фосфата (PO43-). В этом случае, каждый ион кальция имеет заряд +2, а каждый ион фосфата имеет заряд -3. Для баланса зарядов нужно 3 иона кальция и 2 иона фосфата. В итоговой формуле слева от скобок присутствует префикс "три" в обозначении кальция, а справа - цифра "два" перед ионом фосфата, чтобы указать соответствующую стехиометрию.
Фосфаты металлов натрия и кальция имеют различные применения. Натриевый фосфат используется в фармацевтической и пищевой промышленности как добавка в пищевые продукты и лекарственные препараты. Кальциевый фосфат, в свою очередь, широко применяется в производстве удобрений, строительных материалов и стекла.
Фосфат натрия (Na3PO4)
Фосфат натрия (Na3PO4) - это неорганическое соединение, состоящее из ионов натрия (Na+) и ионов фосфата (PO43-). Оно обладает сильной алкалической реакцией и широко используется в различных отраслях промышленности и науки.
Структура фосфата натрия базируется на трех атомах натрия и одном атоме фосфора. Фосфор и атомы натрия связаны между собой посредством ковалентной и ионной связи. Каждый атом фосфора образует четыре связи с различными атомами кислорода, образуя ион фосфата. Соединение имеет кристаллическую структуру и образует укладку в виде трехмерной решетки.
Фосфат натрия широко применяется в производстве стекла, моющих средств, чистящих порошков, удобрений и многих других продуктов. В стекловарении он используется в качестве компонента для изменения химических и физических свойств стекла. Кроме того, фосфат натрия является эффективным моющим средством, которое способно удалять грязь, жиры и другие загрязнения.
Использование фосфата натрия в сельском хозяйстве позволяет улучшить плодородие почвы и увеличить урожайность растений. Фосфат натрия обладает высокой растворимостью в воде, что позволяет растениям эффективно усваивать фосфор, необходимый для их нормального роста и развития. Он также может использоваться в качестве аддитива в пищевой промышленности для регулирования кислотности и улучшения вкусовых качеств продуктов.
В заключение, фосфат натрия (Na3PO4) является важным неорганическим соединением, которое широко применяется в различных отраслях промышленности и науки. Его свойства и структура делают его незаменимым ингредиентом для производства стекла, моющих средств, удобрений и других продуктов. Кроме того, он играет важную роль в сельском хозяйстве, улучшая плодородие почвы и увеличивая урожайность растений.
Формула и структура фосфата натрия
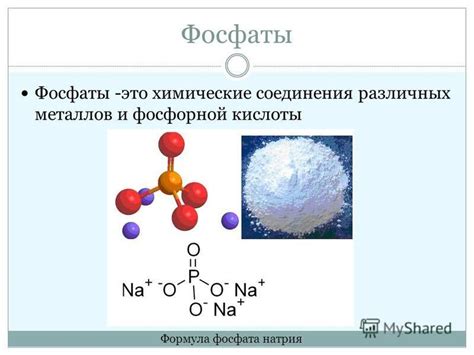
Фосфат натрия (Na3PO4) представляет собой химическое соединение, состоящее из трех ионов натрия (Na+) и одного иона фосфата (PO43-). Это бинарная соль, получаемая путем реакции натрия с фосфорной кислотой или фосфатными растворами.
Структура фосфата натрия является ионной, где ионы натрия и ионы фосфата образуют регулярную кристаллическую решетку. В кристаллической решетке ионы натрия окружают ионы фосфата и удерживают их в стабильном положении.
Фосфат натрия является белым кристаллическим порошком, растворимым в воде. Он обладает особыми свойствами, такими как антиоксидантные и стабилизирующие эффекты, что делает его полезным в различных промышленных и медицинских приложениях.
Объяснение формулы фосфата натрия
Фосфат натрия - это химическое соединение, состоящее из атомов фосфора (P), натрия (Na) и кислорода (O). Его формула обычно записывается как Na3PO4.
Фосфат натрия является солью, образованной отрицательными и положительными ионами. В данном случае, ионы фосфора и натрия привлекаются друг к другу с помощью ионной связи.
Фосфатный ион (PO4^3-) является отрицательно заряженным, а натрий (Na+) - положительно заряженным. В молекуле фосфата натрия имеет место сращение трех ионов натрия с одним ионом фосфата.
Эта формула указывает, что в одной молекуле фосфата натрия присутствуют три иона натрия и один ион фосфата. Ионы натрия необходимы для компенсации отрицательного заряда фосфата, в результате чего образуется устойчивое нейтральное соединение.
Фосфат натрия часто используется в пищевой промышленности для регулирования pH, эмульгации, стабилизации и консервации продуктов. Он также используется в лаборатории в качестве реагента для анализа и синтеза соединений.
Фосфат кальция (Ca3(PO4)2)
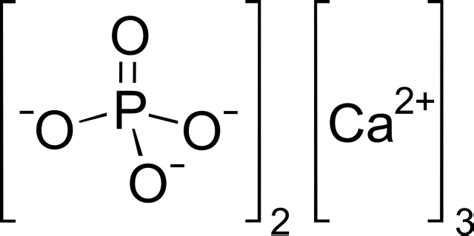
Фосфат кальция (Ca3(PO4)2) является одним из основных соединений фосфора и кальция. Он представляет собой белый кристаллический порошок, который обладает высокой растворимостью в кислотах.
Формула фосфата кальция представляет собой множество катионов кальция (Ca2+) и анионов фосфата (PO43-). Каждый ион кальция связан с двумя ионами фосфата, образуя структуру с высокой степенью структурного порядка. Вещество образует кристаллы с простыми симметричными формами и обладает высокими механическими свойствами.
Фосфат кальция широко используется в медицине и биологии благодаря своим уникальным свойствам. Он является неорганическим источником фосфора и кальция, необходимых для строительства костей и зубов. Кроме того, он используется в качестве добавки в пищу и промышленности для улучшения качества продуктов и материалов.
Фосфат кальция является основной составляющей костной ткани и зубной эмали. Он обладает высокой биосовместимостью и не вызывает аллергических реакций, поэтому широко применяется в хирургии и стоматологии для изготовления имплантатов и протезов. Благодаря своей структуре и свойствам, фосфат кальция способствует быстрому росту костей и восстановлению тканей.
Формула и структура фосфата кальция
Фосфат кальция – это неорганическое соединение, в котором кальций сочетается с фосфорной кислотой. Его химическая формула Ca3(PO4)2 показывает, что в молекуле фосфата кальция содержится 3 атома кальция и 2 группы фосфатных ионов.
Структура фосфата кальция образуется благодаря взаимодействию положительно заряженных ионов кальция с отрицательно заряженными группами фосфатных ионов. При этом каждый фосфатный ион содержит один атом фосфора, связанный с четырьмя атомами кислорода и образующий пирамидальную структуру.
Фосфат кальция обычно присутствует в природе в виде минерала апатита, который имеет кристаллическую структуру. Структура апатита состоит из кристаллической решетки, в которую входят ионы кальция и фосфатные группы. Эти группы образуют шестиугольные кольца, вокруг которых находятся ионы кальция.
Фосфат кальция широко используется в промышленности, а также в медицине. В промышленности его применяют в производстве удобрений, стекла, керамики и других материалов. В медицине он используется для производства лекарственных препаратов, а также в качестве добавки в пищу для укрепления костной ткани.
Таким образом, формула и структура фосфата кальция являются основой его химических свойств и определяют его применение в различных областях науки и промышленности.
Объяснение формулы фосфата кальция
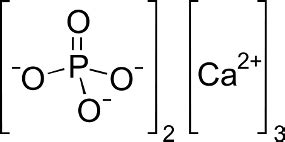
Фосфат кальция – это неорганическое соединение, в котором атомы фосфора образуют соединение с атомами кальция. Формула фосфата кальция обозначается как Ca3(PO4)2.
В формуле указано, что в молекуле фосфата кальция содержится три атома кальция и два иона фосфата. Кальций, обозначаемый символом Ca, образует положительные ионы и является металлом из группы 2 периодической таблицы.
Ионы фосфата обозначаются символом PO4 и имеют отрицательный заряд. Фосфат ионы состоят из одного атома фосфора, образующего связь с четырьмя атомами кислорода. Таким образом, один ион фосфата состоит из шести атомов.
Кальций образует три положительных иона, чтобы скомпенсировать два отрицательных иона фосфата. Соединение этих ионов образует структуру октаэдра, где ионы кальция находятся в центре, а ионы фосфата окружают их со всех сторон.
Фосфат кальция широко используется в промышленности, а также в медицине и сельском хозяйстве. Он является одним из основных компонентов костей и зубов, обеспечивает крепкость их структуры. Также фосфат кальция применяется в производстве удобрений, стекла, керамики и лекарственных препаратов.
Вопрос-ответ
Какая формула у фосфата натрия?
Формула фосфата натрия — Na₃PO₄. Это соединение образуется в результате реакции натрия (Na) с фосфорной кислотой (H₃PO₄). В молекуле фосфата натрия три атома натрия связаны с атомом фосфора и четырьмя атомами кислорода.
Какая формула у фосфата кальция?
Формула фосфата кальция — Ca₃(PO₄)₂. Это соединение также образуется в результате реакции кальция (Ca) с фосфорной кислотой (H₃PO₄). В молекуле фосфата кальция три атома кальция связаны с двумя группами фосфорной кислоты и четырьмя атомами кислорода.
Можно ли использовать фосфат кальция в пищевых продуктах?
Да, фосфат кальция допускается к использованию в пищевых продуктах. Он добавляется, например, в молочные продукты, чтобы улучшить текстуру, а также в кисломолочные напитки, чтобы предотвратить оседание сыроватки. Кроме того, фосфат кальция является хорошим источником кальция, который необходим для здоровья костей и зубов.

